第一章 单元测试
1、单选题:
一定量气体在一定压力下,当温度由100℃上升至200℃时,则气体 ( )。
选项:
A:体积减小但并非减小一半
B:体积减小一半
C:体积增加但并非增加一倍
D:体积增加一倍
答案: 【体积增加但并非增加一倍】
2、单选题:
气体处于那种状态下更接近理想气体?( )。
选项:
A:高压低温
B:低压低温
C:低压高温
D:高压高温
答案: 【低压高温】
3、单选题:
将一定量的N2和一定量的He 放在一个密闭容器中混合均匀,在温度不变时,此混合气体的总压力为 ( )
选项:
A:N2 单独占有此容器时的压力
B:混合前N2和He 压力之和。
C:N2和He 分别占有此容器时压力之和
D:He 单独占有此容器时的压力
答案: 【N2和He 分别占有此容器时压力之和】
4、单选题:
测定人血清白蛋白(HSA)摩尔质量的最好方法是( )。
选项:
A:蒸气压下降法
B:凝固点下降法
C:渗透压法
D:沸点升高法
答案: 【渗透压法】
5、单选题:
同温度下, 渗透压最大的水溶液是 ( )。
选项:
A:0.01 mol·kg-1 HCOOH
B:0.01 mol·kg-1 KNO3
C:0.01 mol·kg-1蔗糖溶液
D:0.01 mol·kg-1 Ba(NO3)2
答案: 【0.01 mol·kg-1 Ba(NO3)2】
6、单选题:
在一定温度和压力下,两种不同气体具有相同体积,则这两种气体( )。
选项:
A:密度相同
B:分子数相同
C:分子量相同
D:质量相同
答案: 【分子数相同】
7、单选题:
空气中O2和N2的体积分数分别是21%和79%,若将一定质量的空气压缩到压力为1500KPa,则空气中O2的分压最接近( )
选项:
A:920 KPa
B:315 KPa
C:210 KPa
D:1185 KPa
答案: 【315 KPa】
8、单选题:
取两小块冰(0 ℃),分别放在0 ºC的纯水和盐水中,将会产生的现象是( )。
选项:
A:放在纯水和盐水中的冰都不融化
B:放在盐水中的冰融化,放在纯水中的冰不融化
C:放在纯水中的冰融化,放在盐水中的冰不融化
D:放在纯水和盐水中的冰都融化
答案: 【放在盐水中的冰融化,放在纯水中的冰不融化】
9、判断题:
稀溶液具有共同的性质规律,如溶液的蒸汽压下降、沸点升高、凝固点下降和渗透压等,溶液越稀,其依数性的规律性越强。 ( )
选项:
A:对
B:错
答案: 【对】
10、判断题:
难挥发非电解质稀溶液的依数性不仅与溶质种类有关,而且与溶液的浓度成正比 ( )
选项:
A:对
B:错
答案: 【错】
第二章 单元测试
1、单选题:
已知在恒压下反应C(s)+1/2 O2(g)CO(g)为放热反应,则该反应( )。
选项:
A:U>0, W>0
B:U0
C:U>0, W<0
D:U<0, W<0
答案: 【U<0, W<0】
2、单选题:
CaO( s ) + H2O( l ) = Ca(OH) 2 (l) 在25℃ 及标准状态下反应自发进行, 高温时其逆反应自发, 这表明该反应为哪种类型 ( )。
选项:
A:Δr Hm > 0, Δr Sm > 0
B:Δr Hm r Sm < 0
C:Δr Hm r Sm > 0
D:Δr Hm > 0, Δr Sm < 0
答案: 【Δr Hm r Sm < 0】
3、单选题:
如果某一体系从状态A变到状态B有两种途径: 一种是经C到B 状态; 另一种是经D到E, 最后到B状态。 体系内能的改变值为( )。
选项:
A:△U = UB -UA
B:△U<0
C:△U > 0
D:△U = 0
答案: 【△U = UB -UA】
4、单选题:
下列有关热效应的正确说法是( )。
选项:
A:石墨始终在298K 温度下燃烧放出的热量
B:其焓变值是人为规定的
C:石墨燃烧后, 使CO2的温度恢复到石墨燃烧时的起始温度, 并只做体积功
D:石墨与CO2在燃烧温度时的热效应
答案: 【石墨燃烧后, 使CO2的温度恢复到石墨燃烧时的起始温度, 并只做体积功】
5、单选题:
如果体系经过一系列变化最后又回到初始状态, 则体系的( )。
选项:
A:Q≠0 W≠△0 U=0 △H=Q
B:Q =-W △U=Q+W △H=0
C:Q=0 W=0 △U=0 △H=0
D:Q≠W △U=Q+W △H=0
答案: 【Q =-W △U=Q+W △H=0】
6、单选题:
根据熵变的概念,判断下列哪反应在室温条件下,正向反应熵变数值最大( )。
选项:
A:CH4(g) → C(s) + 2H2 (g)
B:CaCO3(s) → CaO(s) + CO2(g)
C:2NH3(g) → 3H2(g) + N2(g)
D:H2O(l) → 2H2(g) + 1/2O2(g)
答案: 【2NH3(g) → 3H2(g) + N2(g)】
7、判断题:
任何一个反应不论在什么条件下进行, 如果△rG大于零,则该反应一定不能正向进行。 ( )
选项:
A:对
B:错
答案: 【错】
8、判断题:
反应的热效应就是反应的焓变。( )
选项:
A:对
B:错
答案: 【错】
9、判断题:
化学反应的热效应是指某化学反应从始态到终态的等温变化 过程中(只做体积功),体系与环境所交换的能量。( )
选项:
A:对
B:错
答案: 【错】
10、判断题:
过程是始态到终态的一个变化,途径是实施过程的具体步骤。( )
选项:
A:对
B:错
答案: 【对】
第三章 单元测试
1、单选题:
某温度下, A + B2C反应达到平衡,若增大或减少B的量,C和A的平衡浓度都不变, 则B是 ( )。
选项:
A:气体
B:溶液
C:其它选项都正确
D:纯固体或纯液体
答案: 【】
2、单选题:
某一温度时, 当反应2SO2(g) + O2(g) ←→ 2SO3(g) 达平衡时,是指( )。
选项:
A:SO2, O2, SO3浓度相等
B:2mol SO2和1mol O2反应, 生成2 mol SO3
C:SO2和O2生成SO3的速度等于SO3分解的速度
D:SO2不再发生反应
答案: 【
3、单选题:
若有一可逆反应2A(g) + 2B(g) ←→ C(g) + 2D(g) △H< 0, A, B 有最大转化率的条件( )。
选项:
A:高温高压
B:低温高压
C:高温低压
D:低温低压
答案: 【
4、单选题:
在生产中, 化学平衡原理应用于( )。
选项:
A:反应速率不很慢的反应
B:处于平衡状态的反应
C:一切化学反应
D:恒温下的反应.
答案: 【
5、单选题:
正反应和逆反应的平衡常数之间的关系是( )。
选项:
A: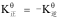
B: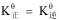
C: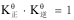
D: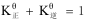
答案: 【
6、单选题:
温度一定时,减小生成物浓度,该反应 ( )。
选项:
A:正反应速率减小
B:正反应速率增大
C:平衡常数减小
D:平衡常数不变
答案: 【
7、单选题:
下列关于反应商Q的叙述中错误的是( )。
选项:
A:Q的数值随反应的进行而变化
B:Q既可能大于K θ,也可能小于K θ
C:Q与 K θ 的数值始终相等
D:Q有时等于K θ
答案: 【】
8、判断题:
反应2A(g) + B(g) ←→ 2C(g), △H 2/([A]2[B]), 随着反应的进行, 而A 和B 的浓度减少, 故平衡常数K增大。( )
选项:
A:错
B:对
答案: 【】
9、判断题:
化学平衡常数是化学反应本质决定的, 因此与反应的条件无关。( )
选项:
A:对
B:错
答案: 【】
10、判断题:
溶度积小的, 不能认为溶解度也一定小, 故溶度积不能反映难溶化合物的溶解能力。( )
选项:
A:错
B:对
答案: 【】
第四章 单元测试
1、单选题:
在298 K 100 mL 0.10 mol/L HAc溶液中, 加入1克NaAc后, 溶液的pH 值( )。
选项:
A:升高
B:降低
C:不变
D:不能判断
答案: 【】
2、单选题:
Ag2CrO4在0.0010 mol·dm-3 AgNO3溶液中的溶解度较在0.0010 mol·dm-3 K2CrO4中的溶解度 ( )。
选项:
A:可能大也可能小
B:相等
C:小
D:大
答案: 【】
3、单选题:
按酸碱质子理论考虑,在水溶液中既可作酸亦可作碱的物质是( )。
选项:
A:H3O+
B:HCO3-
C:C1-
D:NH4+
答案: 【】
4、单选题:
在0.10 L 0.10 mol•L-1 HAc溶液中,加入0.10 mol NaCl晶体,溶液的pH值将会 ( )。
选项:
A:无法判断
B:不变
C:升高
D:降低
答案: 【
5、单选题:
已知体积为V1, 浓度为0.2 mol/L弱酸溶液, 若使其解离度增加一倍, 则溶液的体积V2应为 ( )。
选项:
A:10V1
B:4V1
C:3V1
D:2V1
答案: 【】
6、单选题:
欲配置pH=5的缓冲溶液,应选用的缓冲对为( )。
选项:
A:HAc-Ac- (PKa = 4.75)
B:HPO42--PO43- (PKa = 12.32)
C:HSO3--SO32- (PKa = 7.2)
D:HCO3--CO32- (PKa = 10.33)
答案: 【
7、单选题:
依软硬酸碱概念,下列物质属于软酸的是 ( )。
选项:
A:NH3
B:AsH3
C:Ag+
D:H+
答案: 【】
8、判断题:
稀释可以使醋酸的电离度增大, 因而可使其酸度增强。( )
选项:
A:对
B:错
答案: 【】
9、判断题:
溶液中若不存在同离子效应, 也就不会构成缓冲溶液。( )
选项:
A:错
B:对
答案: 【
10、判断题:
酸碱反应到达终点后溶液的pH呈中性。( )
选项:
A:错
B:对
答案: 【】
第五章 单元测试
1、单选题:
已知:E(Sn4+/Sn2+) = + 0.15 V,E(Fe3+/Fe2+) = + 0.77 V,则不能共存于同一溶液中的一对离子是 ( )。
选项:
A:Sn4+, Sn2+
B:Fe3+, Fe2+
C:Fe3+, Sn2+
D:Sn4+, Fe2+
答案: 【
2、单选题:
与下列原电池电动势无关的因素有 (-)Zn | ZnSO4(aq)║HCl(aq)|H2(101 325 Pa), Pt(+) ( )。
选项:
A:温度
B:氢的体积
C:ZnSO4浓度
D:盐酸浓度
答案: 【
3、单选题:
原电池中关于盐桥的说法不正确的是 ( )。
选项:
A:盐桥可以没有
B:中和两个半电池中的电荷
C:内装有饱和KCl和琼胶做成的冻胶
D:形成闭合回路
答案: 【
4、单选题:
Na2S4O6中S的氧化数是( )。
选项:
A:3
B:0
C:2.5
D:5
答案: 【】
5、单选题:
关于标准电极电势说法正确的是( )。
选项:
A:标准电极电势与温度无关。
B:标准电极电势的数值与电对得失电子数有关系。
C:可以根据标准电极电势的数值判断物质的氧化性和还原性的相对强弱。
D:所有电对的标准电极电势都可以与标准氢电极构成原电池而测到。
答案: 【】
6、单选题:
原电池中负极发生( )。
选项:
A:氧化还原反应
B:其它选项都不对
C:非氧化还原反应
D:氧化反应
答案: 【
7、单选题:
氧化还原反应中氧化数升高的称为 ,氧化数降低的称为 。 ( )
选项:
A:氧化剂、还原剂
B:还原剂、还原剂
C:氧化剂、氧化剂
D:还原剂、氧化剂
答案: 【
8、判断题:
能组成原电池的反应都是氧化还原反应。( )
选项:
A:错
B:对
答案: 【】
9、判断题:
标准电极电势的数值越小, 其氧化型的氧化性越弱, 其还原型的还原性越强。( )
选项:
A:对
B:错
答案: 【】
10、判断题:
在一个能实际产生电流的原电池中, 作为正极的电极反应的电势总是高于作为负极的电极反应的电势值。( )
选项:
A:错
B:对
答案: 【】
第六章 单元测试
1、单选题:
波函数和原子轨道二者之间的关系是 ( )。
选项:
A:另外三种说法都不对
B:波函数和原子轨道是同义词
C:只有轨道波函数与原子轨道才是同义的
D:波函数是函数式, 原子轨道是电子轨迹
答案: 【
2、单选题:
多电子原子的原子轨道能级顺序随着原子序数的增加( )。
选项:
A:轨道能量逐渐降低, 能级顺序也会改变
B:轨道能量逐渐增加, 能级顺序不变
C:轨道能量逐渐降低, 但能级顺序不变
D:轨道能量基本不变, 但能级顺序改变
答案: 【
3、单选题:
同一原子中, 可能存在下列量子数的两个电子是( )。
选项:
A:(2, 0, 1, +1/2) 和 (2, 0, 1, -1/2)
B:(1, 0, 0,-1/2) 和 (1, 0, 0, -1/2)
C:(3, 2, 0, -1/2) 和 (3, 2, 1,-1/2)
D:(1, 1, 0, +1/2) 和 (1, 1, 0, -1/2)
答案: 【
4、单选题:
下列电子构型中,电离能最低的是( )。
选项:
A:ns2np4
B:ns2np3
C:ns2np6
D:ns2np5
答案: 【
5、单选题:
下列原子参数与元素周期性变化的说法不正确的是 ( )。
选项:
A:同周期相邻元素原子半径的减小幅度:主族> 过渡> 内过渡
B:随着原子序数的增大, 原子半径自左至右减小
C:同族元素电离能的趋势:自上至下减小,与原子半径增大的趋势刚好相反
D:同周期元素电离能变化趋势:自左至右增大,与原子半径减小的趋势一致
答案: 【
6、单选题:
在一个多电子原子中,具有下列各套量子数的电子,能量大的电子具有的量子数(n, l, m, mS) 是 ( )。
选项:
A:(3, 1,-1,+1/2)
B:(3,2,+1,+1/2)
C:(2,1,+1,-1/2)
D:(3,1,,0,-1/2)
答案: 【
7、单选题:
p轨道的简并度为 ( )。
选项:
A:2
B:1
C:4
D:3
答案: 【】
8、判断题:
所有微观粒子都既有粒子性又有波动性。( )。
选项:
A:对
B:错
答案: 【
9、判断题:
对于同一原子, 失去同层电子时电离能差值较小,而失去不同层电子时电离能差值较大。所以电离能数据也是原子核外电子分层排布的实验佐证。( )。
选项:
A:错
B:对
答案: 【】
10、判断题:
原子失去电子变成简单阳离子时,失电子顺序与电子填充顺序正好相反。( )。
选项:
A:对
B:错
答案: 【】
第七章 单元测试
1、单选题:
关于晶格能, 下列说法中正确的是( )。
选项:
A:晶格能是指气态阳离子与气态阴离子生成离子晶体所释放的能量
B:晶格能是由单质化合成1 mol离子化合物时所释放的能量
C:晶格能是指气态阳离子与气态阴离子生成1 mol离子晶体所释放的能量
D:晶格能就是组成离子晶体时, 离子键的键能
答案: 【
2、单选题:
乙炔分子(C2H2)中, 碳原子采取的是( )。
选项:
A:sp杂化
B:不等性sp3杂化
C:等性sp3杂化
D:sp2杂化
答案:
3、单选题:
乙醇和醋酸易溶于水, 而碘和二硫化碳难溶于水的原因是 ( )。
选项:
A:分子量不同
B:有无氢键
C:分子间力不同
D:分子的极性不同
答案: 【
4、单选题:
按VSEPR理论, BrF3分子的空间几何构型为( )。
选项:
A:三角双锥形
B:平面三角形
C:T形
D:三角锥形
答案:
5、单选题:
H2S分子与CH4分子间存在的分子间力有( )。
选项:
A:取向力,色散力,诱导力
B:取向力,色散力
C:取向力,诱导力
D:诱导力,色散力
答案: 【
6、单选题:
下列说法中,正确的是( )
选项:
A:阴离子总是比阳离子大
B:离子键和共价键相比,其作用范围更大
C:离子型固体的饱和水溶液导电性都极其良好
D:所有高熔点物质都是离子型的
答案: 【
7、多选题:
冰融化所克服作用力有 ( )
选项:
A:诱导力
B:氢键
C:取向力
D:色散力
答案: 【】
8、判断题:
CO2 分子空间构型为直线型,是非极性分子,其化学键也是非极性的。( )
选项:
A:错
B:对
答案: 【】
9、判断题:
当2个原子形成共价键时, 可以是σ加π键, 也可以都是σ键。( )。
选项:
A:错
B:对
答案: 【】
10、判断题:
O2+的键级是2.5,O2的键级是2.0,所以O2+比O2更稳定。( )
选项:
A:错
B:对
答案: 【】
第八章 单元测试
1、单选题:
某配合物组成为Co(NH3)5BrSO4 , 加入BaCl2 时产生沉淀 , 加入AgNO3时不产生沉淀,则 该化合物的化学式为 ( )。
选项:
A:[Co(NH3)5Br]SO4
B:[Co(NH3)5SO4]Br
C:[Co(NH3)5BrSO4]
D:[Co (NH3)5]BrSO4
答案: 【
2、单选题:
配合物中心离子的配位数等于( )。
选项:
A:配位原子中的孤对电子数
B:配位体中的原子数
C:配位原子数
D:配位体数
答案: 【
3、单选题:
在[ Co( NH3)3(H2O)2Cl]2+中, (Co )的氧化数和配位数分别为( )。
选项:
A:+ 2 和4
B:+ 2 和6
C:+ 3 和6
D:+ 3 和4
答案:
4、单选题:
下列配合物中属于内轨型的是( )。
选项:
A:[ FeF6 ]3-
B:[ Fe(CN)6 ]3-
C:[ Fe(H2O)6 ]3+
D:[Fe(H2O)6 ]2+
答案: 【
5、单选题:
关于外轨型与内转型配合物的区别,下列说法不正确的是( )。
选项:
A:中心离子轨道杂化方式在外轨型配合物是ns、np、nd轨道杂化,内轨型配合物是(n-1)d、ns、np轨道杂化
B:通常外轨型配合物中配位原子的电负性比内轨型配合物中配位原子的电负性大
C:一般外轨型配合物比内轨型配合物键能小,内轨型配合物具有较大的稳定性。
D:通常外轨型配合物比内轨型配合物磁矩小
答案: 【
6、单选题:
[Cr(Py)2(H2O)Cl3]中Py代表吡啶, 这个化合物的名称是( )。
选项:
A:二吡啶一水三氯化铬(Ⅲ)
B:三氯一水二吡啶合铬(Ⅲ)
C:一水合三氯化二吡啶合铬(Ⅲ)
D:三氯化一水二吡啶合铬(Ⅲ)
答案: 【
7、判断题:
配位原子与中心原子之间的化学键也有可能是多重键。( )。
选项:
A:对
B:错
答案: 【】
8、判断题:
配合物都包含有内界和外界两部分。( )
选项:
A:对
B:错
答案: 【
9、判断题:
配位键没有方向性和饱和性。( )
选项:
A:对
B:错
答案: 【】
10、判断题:
配合物中, 中心离子一般为正价态和零价态金属离子, 而配体一般为含有电负性比较高的负离子或中性分子。( )
选项:
A:错
B:对
答案: 【】
第九章 单元测试
1、单选题:
下列不属于系统误差的是 ( )。
选项:
A:天平的砝码被腐蚀了
B:配制溶液的蒸馏水含有少量杂质
C:实验时滴定管的读数不准
D:某同学实验数据总是偏高
答案: 【
2、单选题:
分析天平称量的样品质量为0.3556g,假定其真值为0.3559g,测定的相对误差为 ( )。
选项:
A:-0.08%
B:0.15%
C:0
D:-0.15%
答案: 【
3、单选题:
标定HCl时最好选择的基准物质是( )。
选项:
A:NaOH
B:Na2B4O7·10H2O
C:Na2CO3
D:邻苯二甲酸氢钾
答案: 【
4、单选题:
如果要求分析结果的相对误差小于0.1%,若称量的绝对误差为±0.2mg,则称取样品的质量至少应为 ( )。
选项:
A:0.1g
B:0.2g
C:0.01g
D:0.02g
答案: 【
5、单选题:
pH = 2 .300 的有效数字位数是( )。。
选项:
A:1 位
B:3 位
C:4 位
D:2 位
答案: 【
6、单选题:
有一碱液, 可能含有NaOH, Na2CO3 , NaHCO3 , 今以盐酸滴定之, 先以酚酞为指示剂, 消耗盐酸的体积为V1 , 再以甲基橙为指示剂, 消耗盐酸体积为V2 , 且有V1 > V2 , 问该碱液的组成为( )。
选项:
A:NaOH + Na2CO3
B:NaOH + NaHCO3
C:NaHCO3 + Na2CO3
D:Na2CO3
答案: 【
7、单选题:
在定量分析中,精密度与准确度之间的关系是( )。
选项:
A:准确度是保证精密度的前提
B:精密度高,准确度必然高
C:精密度是保证准确度的前提
D:准确度高,精密度必然高
答案: 【】
8、判断题:
做对照实验和空白实验,校正仪器和方法都可以减免和消除系统误差。( )
选项:
A:对
B:错
答案: 【】
9、判断题:
实验中三次平行测定的结果越接近,说明测定的准确度越高。( )
选项:
A:错
B:对
答案: 【】
10、判断题:
仪器能测量得到的数字就是有效数字。( )
选项:
A:对
B:错
答案: 【】
第十章 单元测试
1、单选题:
滴定反应对化学反应的要求不包括 ( )。
选项:
A:定量进行,通常要求达到99.9%以上
B:不存在干扰杂质
C:较快的反应速度,或有简便方法(加热、加催化剂)加速反应
D:具有确定的计量关系
答案: 【
2、单选题:
用0.1000 mol/L的NaOH标准溶液滴定0.1000 mol/L的HAc溶液,其突跃范围pH = 7.76~9.70, 应选用哪一指示剂?( )。
选项:
A:酚酞(pH = 8.0~10.0)
B:中性红(pH = 6.8~8.0)
C:甲基橙(pH = 3.1~4.4)
D:甲基红(pH = 4.4~6.2)
答案: 【
3、单选题:
酸碱滴定中,选择指示剂可不必考虑的因素是( )。
选项:
A:指示剂的颜色变化
B:指示剂的分子结构
C:指示剂的变色范围
D:pH突跃范围
答案: 【
4、单选题:
用EDTA直接滴定有色金属离子,终点所呈现的颜色是( )。
选项:
A:B和C的混合物颜色
B:EDTA-金属离子配合物的颜色
C:游离指示剂的颜色
D:指示剂-金属离子配合物的颜色
答案: 【
5、单选题:
比较下列滴定,哪类类型滴定突跃最大( )
选项:
A:0.10 mol/dm-3滴定0.10 mol/dm-3 HCl
B:0.10 mol/dm-3滴定0.10 mol/dm-3 HCOOH
C:1.0 mol/dm-3滴定1.0 mol/dm-3 HCl
D:0.10 mol/dm-3滴定0.10 mol/dm-3HAc
答案: 【
6、单选题:
用已知浓度的NaOH滴定相同浓度的不同弱酸时,弱酸的pKa 越大,则( )。
选项:
A:滴定突跃越大
B:消耗的NaOH的量越多
C:滴定终点时指示剂颜色变化也不明显
D:滴定突跃越小
答案: 【
7、判断题:
若采用含有少量中性杂质的H2C2O42H2O作为基准标定NaOH溶液的浓度,会使得标定结果偏低( )。
选项:
A:对
B:错
答案: 【】
8、判断题:
Ca2+,Mg2+离子共存时,可以通过控制溶液pH值对Ca2+,Mg2+离子进行分别滴定 ( )。
选项:
A:错
B:对
答案: 【】
9、判断题:
金属指示剂与金属离子生成的配合物越稳定,滴定准确度越高( )。
选项:
A:对
B:错
答案: 【
10、判断题:
EDTA滴定中消除共存离子最有效的方法是分离干扰离子( )
选项:
A:错
B:对
答案: 【】


请先 !