第一章 单元测试
1、判断题:
无机及分析化学就是将无机化学和分析化学有机整合,集二者的基础性和实用性于一身的一门化学专业基础课程,是大学化学的基石和化学研究的起点。
选项:
A:对
B:错
答案: 【对】
2、判断题:
用已知浓度的氯化钡溶液测定硫酸根的含量,可采用重量分析法。
选项:
A:对
B:错
答案: 【对】
3、判断题:
从历史上看,无机化学是发展最早的一门化学分支学科,是化学研究的先驱。
选项:
A:对
B:错
答案: 【对】
4、单选题:
以化学反应为基础的分析方法,称为:
选项:
A:
仪器分析法
B:
化学分析法
答案: 【
化学分析法
】
5、多选题:
通常所说的四大化学是指?
选项:
A:无机及分析化学
B:
无机化学
C:
有机化学
D:
分析化学
E:
物理化学
答案: 【
无机化学
;
有机化学
;
分析化学
;
物理化学
】
6、多选题:
本课程包含化学的哪两个二级学科?
选项:
A:
无机化学
B:
分析化学
C:
物理化学
D:
有机化学
答案: 【
无机化学
;
分析化学
】
7、多选题:
下列哪些内容属于无机化学的研究对象?
选项:
A:
化学热力学
B:
化学动力学
C:
配位化学
D:
元素化学
E:
电化学
F:
结构化学
答案: 【
化学热力学
;
化学动力学
;
配位化学
;
元素化学
;
电化学
;
结构化学
】
第二章 单元测试
1、多选题:
已知置信度为90%,n = 6 时,t = 2.015,在一组平行测定中, 所得测定结果如下: 8.44, 8.32, 8.45, 8.52, 8.69, 8.38,下列内容正确的是
选项:
A:置信度为90%时平均值的置信区间8.47±0.11
B:标准偏差为0.13
C:相对平均偏差为0.11%
答案: 【置信度为90%时平均值的置信区间8.47±0.11;标准偏差为0.13】
2、单选题:
已知n = 6 时,Q0.90 = 0. 56。在一组平行测定中,所得测定结果如下: 10.56,10.44,10.57,10.64,10.81,10.50,则
选项:
A:
所有数据都是可靠值
B:
10.44是可疑值
C:
10.81是可疑值
答案: 【
所有数据都是可靠值
】
3、判断题:
系统误差具有重现性,是可测误差
选项:
A:对
B:错
答案: 【对】
4、判断题:
由于偶然误差所得到数据,不能参加平均值的计算
选项:
A:对
B:错
答案: 【错】
5、判断题:
滴定分析中所选择的终点指示剂确定的终点和理论终点不一致,由此造成的误差主要是试剂误差。
选项:
A:对
B:错
答案: 【错】
6、判断题:
系统误差主要影响分析测定中的准确度
选项:
A:错
B:对
答案: 【对】
7、判断题:
pM=-lg[Mn+]=3.00,金属离子浓度[Mn+]有效数字位数为3位
选项:
A:错
B:对
答案: 【错】
8、判断题:
对于同一组测定数据,置信度越小,置信区间越小。
选项:
A:对
B:错
答案: 【对】
9、单选题:
用分析天平采用减量法称量试样,要使称量误差不大于0.1%,至少要称取试样
选项:
A:0.2g
B:2.0g
C:1.0g
D:0.1g
答案: 【0.2g】
10、判断题:
已知 pH=5.25,则[ H+ ]=5.62×10-6mol•L-1 。
选项:
A:对
B:错
答案: 【错】
11、单选题:
按有效数字运算规则:(2.7+5.9)÷lg2.56的结果有效数字位数是
选项:
A:3位
B:4位
C:2位
答案: 【3位】
12、判断题:
按照“四舍六入五成双”的修约规则,把0.411650修约成四位有效数字,应为0.4116
选项:
A:对
B:错
答案: 【对】
13、单选题:
测定一试样中Si的百分含量如下: 20.60%, 20.61%, 20.63%, 20.65%, 20.66%,则其相对平均偏差为(结果保留一位有效数字)。
选项:
A:0.1%
B:0.2%
C:1%
D:0.5%
答案: 【0.1%】
14、单选题:
可用下列哪种方法减小分析测定中的偶然误差
选项:
A:空白实验
B:改进测量方法
C:增加测定次数
D:对照实验
答案: 【增加测定次数】
15、单选题:
按有效数字运算规则:(43.5–35.0)×0.126-0.071的结果是
选项:
A:1.00
B:1.000
C:1.0
D:1
答案: 【1.00】
16、多选题:
下列哪种情况造成的误差属于系统误差( )
选项:
A:滴定管体积读数时最后一位估读
B: 仪器未校准
C:试剂中含有少量被测组分
答案: 【 仪器未校准
;试剂中含有少量被测组分】
第三章 单元测试
1、判断题:
功,热,内能是状态函数。
选项:
A:对
B:错
答案:
2、判断题:
金刚石的标准摩尔生成吉布斯自由能等于零。
选项:
A:对
B:错
答案:
3、判断题:
温度升高可增大可逆反应的正、逆反应速率常数。
选项:
A:错
B:对
答案:
4、判断题:
在可逆反应中,吸热方向的活化能一般大于放热方向的活化能。
选项:
A:错
B:对
答案:
5、判断题:
对于反应前后分子数相等的可逆反应而言,增大或减小总压力对平衡没有影响。
选项:
A:错
B:对
答案:
6、判断题:
催化剂可改变化学反应的活化能,但不会改变反应平衡常数。
选项:
A:对
B:错
答案:
7、单选题:
在298.15K时,ΔbHϴm(F-F)=158kJ·mol–1,ΔbHϴm(N≡N)=946kJ·mol–1,ΔbHϴm(F-N)=272kJ·mol–1,反应3F2(g)+N2(g) = 2NF3(g) 的ΔrHϴm等于
选项:
A:212kJ·mol–1
B:-106kJ·mol–1
C:106kJ·mol–1
D:-212kJ·mol–1
答案:
8、判断题:
在298.15K时:ΔfGϴm,HI(g)= 1.7kJ·mol-1,则反应 H2(g) + I2(s) =2HI(g)的ΔrGϴm=-3.4kJ·mol-1。
选项:
A:对
B:错
答案:
9、单选题:
对于基元反应:2A(g)+B(s)=C(g),在一定温度下,系统压力增加为原来的4倍,则反应速率是原来的
选项:
A:4倍
B:64倍
C:8倍
D:16倍
答案:
10、单选题:
一定温度下,在某容器中注入A2(g)和B2(g),反应发生前,A2(g)和B2(g)的分压为p(A2)=100kPa,p(B2)=200kPa,当反应A2(g)+3B2(g)=2AB3(g)达平衡时,p(AB3) =100kPa,该温度下反应的Kϴ等于
选项:
A:0.0625
B:1.6×10-3
C:16
D:625
答案:
11、单选题:
某反应的△rHϴm(298.15K)=112.6kJ·mol-1,△rSϴm(298.15K)=112.6J.mol-1·K-1,在标准态下该反应能自发进行的最低温度为
选项:
A:10K
B:100K
C:1K
D:1000K
答案:
12、单选题:
某反应500K时△rGϴm(500K)=-316.4kJ·mol-1,该温度下反应的Kϴ等于
选项:
A:1.08
B:1.1×1033
C:1.19
D:8.9×10-34
答案:
13、单选题:
某温度下,反应 1/2A(g)+1/2B(g)=C(g)的Kc=10,则 2C(g)=A(g)+B(g)的 Kc为
选项:
A:0.05
B:20
C:0.01
D:100
答案:
14、单选题:
已知反应A(s)+B(g)=C(g)+D(g)在一定温度下达平衡,若在恒温恒容下引入无关气体,则平衡
选项:
A:向左移动
B:向右移动
C:不移动
答案:
15、多选题:
反应 A(g)+2B(g)=2C(g)在一定温度下达平衡,若其他条件不变,增加系统总压后,下列说法正确的是
选项:
A:反应平衡常数不变
B:反应速率常数增大
C:反应平衡常数增大
D:平衡向右移动
E:反应速率常数不变
答案:
16、单选题:
常温常压下, Zn可溶于盐酸, 其反应的ΔH, ΔS, ΔG应为
选项:
A:
ΔS< 0,ΔH < 0,ΔG< 0
B:
ΔS > 0,ΔH > 0,ΔG< 0
C:
ΔS > 0,ΔH >0,ΔG >0
D:
ΔS > 0, ΔH < 0,ΔG <0
答案:
第四章 单元测试
1、判断题:
0.1M的HAc溶液稀释时,解离度增大,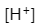 浓度也增大。
浓度也增大。
选项:
A:对
B:错
答案:
2、判断题:
一般来说,酸碱指示剂的变色范围越宽,变色越敏锐。
选项:
A:对
B:错
答案:
3、判断题:
总浓度一定,当缓冲溶液中共轭酸碱的浓度比为1时,缓冲溶液的缓冲能力最大。
选项:
A:对
B:错
答案:
4、单选题:
下列阴离子的水溶液,若浓度(单位  )相同,则何者碱性最强?( )
)相同,则何者碱性最强?( )
选项:
A:
BCN-(KHCN=6.2×10-12)
B:F-(KHF=3.5×10-4)
C:CH3COO-(KHAc=1.8×10-5) E) Cl-(KHCl>>1)
D:S2-(KHS-=7.1×10-15, KH2S=1.3×10-7)
答案:
5、单选题:
下列物质只能是质子碱的是 ( )
选项:
A:CO32-
B:H2O
C:NH4+
D:HS-
答案:
6、单选题:
等浓度的一元弱酸强碱盐溶液 AX,AY,AZ的pH值分别是8,9,10,这三种弱酸的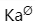 值由大到小的顺序是 ( )
值由大到小的顺序是 ( )
选项:
A:HX>HY>HZ
B:HX>HZ>HY
C:HZ>HY>HX
D:
HZ>HX>HY
答案:
7、单选题:
欲配制pH=9的缓冲溶液,应选用下列何种弱酸或弱碱和它们的(强酸或强碱的)盐来配制( )
选项:
A:NH3·H2O (KbØ=1.8×10-5)
B:NH2OH (KbØ=1.0×10-9)
C:HAc (KaØ=1.8×10-5)
D:HCOOH (KaØ=1.0×10-4) E) HNO2 (KaØ=5×10-4)
答案:
8、单选题:
用纯水把下列溶液稀释10倍时,其中pH值变化最大的是( )
选项:
A:1 mol/L HAc
B:1 mol/L HAc+1 mol/L NaAc
C:1 mol/L NH3·H2O + 1 mol/LNH4Cl
D:0.1mol/L HCl
E:1 mol/L NH3·H2O
答案:
9、单选题:
用HCl标准溶液滴定碳酸盐混合碱液。滴定至酚酞终点时耗去 酸 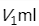 ,从酚酞终点滴定至甲基橙终点时耗去HCl溶液
,从酚酞终点滴定至甲基橙终点时耗去HCl溶液 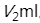 。若混合液中所含的
。若混合液中所含的 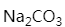 和
和 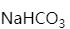 的浓度相等 ,则 ( )
的浓度相等 ,则 ( )
选项:
A:
V1=V2
B:2V1=V2
C:V1=0
D:V1=2V2
答案:
第五章 单元测试
1、判断题:
Kϴsp只与温度有关
选项:
A:错
B:对
答案:
2、判断题:
一定温度下,在难溶电解质的饱和溶液中,Qi = Kϴsp
选项:
A:对
B:错
答案:
3、判断题:
pH越小,难溶弱酸盐的溶解度越小
选项:
A:对
B:错
答案:
4、判断题:
在用BaSO4重量法测定SO42-时,如果BaSO4中有少量PbSO4 ,则测定结果偏高
选项:
A:错
B:对
答案:
5、判断题:
在用BaSO4重量法测定Ba2+时,如果BaSO4中有少量PbSO4 ,则测定结果偏高
选项:
A:对
B:错
答案:
6、判断题:
中性溶液中可以用莫尔法测定Br–
选项:
A:对
B:错
答案:
7、判断题:
测定I-时可用莫尔法直接滴定
选项:
A:对
B:错
答案:
8、单选题:
对于AB2型难溶强电解质,Kϴsp 与溶解度s(mol·L-1)的关系是:Kϴsp 等于
选项:
A:27s4
B:4s3
C:s2
答案:
9、判断题:
在0.010mol·L-1 M2+金属离子溶液中,不断通入H2S气体至饱和,M2+开始沉淀时所需H+浓度为0.32mol∙L-1(已知pKϴsp MS=23.04.,H2S的pKϴa1 =6.89,pKϴa2 =14.15)
选项:
A:对
B:错
答案:
10、判断题:
称量形是Mg2P2O7, 被测组份是P2O5, 换算因数F的表达式为Mg2P2O7/P2O5
选项:
A:错
B:对
答案:
11、单选题:
反应 M2++ H2S = MS + 2H+的 Kϴ等于(已知 pKϴsp MS=19.04, H2S的pKϴa1=6.89,pKϴa2=14.15)
选项:
A:0.5
B:100
C:2
D:0.01
答案:
12、判断题:
用莫尔法测定Cl–,如果指示剂浓度过浓,则测定结果偏低
选项:
A:错
B:对
答案:
13、单选题:
已知CaF2的溶度积 Kϴsp=2.7×10-11,HF的Kϴa=3.5×10-4,则CaF2在保持[H+]=0.35mol•L-1溶液中的溶解度为
选项:
A:3.2×10-3 mol∙L-1
B:2.6×10-3 mol∙L-1
C:1.9×10-2 mol∙L-1
答案:
14、单选题:
已知难溶强电解质 AB, A2B, A3B 的溶度积常数分别为1.6 ×10-11,3.2 ×10-17,2.7 × 10-15 ,溶解度S (mol•L -1)最大的是
选项:
A: A2B
B: A3B
C: AB
答案:
15、多选题:
向金属离子M2+和N2+的混合液中滴加浓NaOH溶液,计算表明: M2+和N2+开始生成氢氧化物沉淀时,所需pH值分别为4.0和6.0, M2+和N2+沉淀完全时,所需pH值分别为5.0和8.0,下列选项正确的是
选项:
A:M2+和N2+分离完全所需要控制的pH值范围是4.0~5.0
B:M2+和N2+分离完全所需要控制的pH值范围是5.0~6.0
C:N2+先沉淀
D:M2+和N2+分离完全所需要控制的pH值范围是6.0~8.0
E:M2+先沉淀
答案:
16、单选题:
下列试剂中使 BaSO4(s)溶解度不变的是
选项:
A:Na2SO4
B: BaCl2
C: H2O
D:NaCl
答案: 【
第六章 单元测试
1、判断题:
离子–电子法应用广泛,适用于所有氧化还原反应方程式的配平。
选项:
A:错
B:对
答案:
2、判断题:
书写原电池符号时,习惯上把负极写在左边,正极写在右边。
选项:
A:对
B:错
答案:
3、判断题:
书写原电池符号时,若电极反应中的物质本身不能作为导电电极,可以用Pb电极作为导电电极。
选项:
A:错
B:对
答案:
4、判断题:
同一电对在不同介质中的电极反应和φϴ值不同。
选项:
A:对
B:错
答案:
5、判断题:
Cu2++ 2e–⇌ Cu 和 2Cu2++4e– ⇌2Cu的φϴ(Cu2+/Cu) 相同。
选项:
A:对
B:错
答案:
6、判断题:
KMnO4标准溶液液可以采用直接法配制。
选项:
A:错
B:对
答案:
7、判断题:
还原电势φϴOx/Red值越大,电对中氧化型物质的氧化能力越强。
选项:
A:对
B:错
答案:
8、判断题:
若增大I– 浓度,则电对CuI/Cu的的电极电势也增大。
选项:
A:错
B:对
答案:
9、单选题:
把反应 2Ag++Cu = Cu2++ 2Ag设计成对应原电池,若在负极中加入Na2S,则原电池电动势
选项:
A:减小
B:不变
C:增大
答案:
10、单选题:
用A4+ 滴定B2+ 时,已知φϴ'(B4+/B2+)=0.16V,φϴ'(A4+/A3+)=1.66V,滴定至化学计量点时的电极电势φsp等于
选项:
A:
1.16V
B:
0.91V
C:
0.66V
答案:
11、判断题:
已知φϴAg+/Ag=0.7999V,φϴAgI/Ag=-0.149V,(忽略离子强度I影响),则KϴspAgI=9.3×10-17
选项:
A:错
B:对
答案:
12、判断题:
已知φϴClO3–/Cl–=1.45V,φϴCl2/ Cl– =1.36V,则φϴClO3–/Cl2= 1.47V
选项:
A:错
B:对
答案:
13、单选题:
已知φϴI2/I–= 0.535V,φϴ Fe3+/Fe2+ = 0.771V,计算表明:反应I2(s)+2Fe2+(0.10mol∙L-1)=2Fe3+(0.010 mol∙L-1)+2I–(0.010mol∙L-1)
选项:
A:
处于平衡状态
B:
逆向进行
C:
正向进行
答案:
14、单选题:
已知:φϴClO3–/Cl– = 1.45 V,φϴClO4–/ClO3–= 1.19 V,298.15K 时反应 4ClO3– = 3 ClO4– + Cl–的 Kϴ 等于
选项:
A:
2.5×104
B:
1.5×1013
C:
2.2×1026
答案:
15、单选题:
已知φϴO2/H2O = 1.229 V,则φϴO2/OH– 等于
选项:
A:
0.216V
B:
0.338
C:
0.400V
答案:
16、单选题:
配平氧化还原反应HClO4 + P4 → HCl +H3PO4 时,需要在反应式的左边添加
选项:
A:10H2O
B:8H2O
C:12H2O
D:14H2O
答案:
17、单选题:
把反应MnO4– + 5Fe2+ + 8H+ = Mn2+ + 5Fe3+ + 4H2O设计成对应原电池,做原电池正极的电对是
选项:
A:MnO4–/ Mn2+
B:MnO4–/ Fe2+
C:Fe3+/ Fe2+
答案:
第七章 单元测试
1、单选题:
下列配合物中,在水溶液中解离度最小的是
选项:
A:
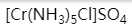
B:
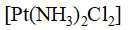
C:
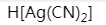
D:
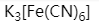
答案:
2、判断题:
在配离子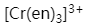 中,形成体是
中,形成体是 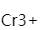 ,配位数为6。
,配位数为6。
选项:
A:错
B:对
答案:
3、判断题:
配合物 中配离子的电荷数为 +2,中心原子为Fe,中心离子的配位数为6 。
中配离子的电荷数为 +2,中心原子为Fe,中心离子的配位数为6 。
选项:
A:对
B:错
答案:
4、判断题:
与一个形成体成键的配体的数目,称为该形成体的配位数。
选项:
A:对
B:错
答案:
5、判断题:
EDTA在水溶液中有七种存在形式,各种存在形式的浓度相对大小取决于溶液的pH值。
选项:
A:对
B:错
答案:
第八章 单元测试
1、单选题:
决定波函数的形状,并在多电子原子中共同决定电子能量的量子数是( )
选项:
A:
n
B:
l
C:
l和m
D:
m
答案:
2、单选题:
下列四个量子数(依次为n,l,m,ms)不合理的一组是:
选项:
A:3、1、0、+ 1/2
B:4、0、0、+1/2
C:2、0、1、-1/2
D:4、3、1、-1/2
答案:
3、判断题:
催化剂能加快反应速率的主要原因是降低了反应活化能,使活化分子分数增大。
选项:
A:对
B:错
答案:
4、判断题:
对于n=4的电子层,可以容纳的轨道数和电子数分别是16和32。
选项:
A:错
B:对
答案:
5、单选题:
利用分子轨道理论判断下列分子键级最小的是
选项:
A:
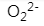
B:
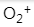
C:
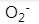
答案:
第九章 单元测试
1、单选题:
下列化合物中既存在离子键和共价键,又存在配位键的是
选项:
A:
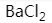
B:

C:

答案:
2、判断题:
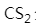 分子空间构型为直线形,是因为C原子采取了sp杂化。
分子空间构型为直线形,是因为C原子采取了sp杂化。
选项:
A:错
B:对
答案:
3、判断题:
用关键词表述原子轨道线性组合秤分子轨道的三个原则对称性一致、能量相近、轨道轨道最大重叠
选项:
A:对
B:错
答案:
4、判断题:
MgO属于离子晶体,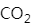 属于子晶体,
属于子晶体,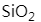 属于原子晶体。
属于原子晶体。
选项:
A:对
B:错
答案:
5、判断题:
判断氨气与水间存在什么形式的分子间作用力氢键与范德华力
选项:
A:对
B:错
答案:
6、判断题:
在化合物分子中,含有极性共价键的分子一定是极性分子,非极性分子中都是非极性共价键。
选项:
A:对
B:错
答案:
7、判断题:
在化合物NaI中,正负离子间存在着附加极化作用。
选项:
A:错
B:对
答案:


请先 !